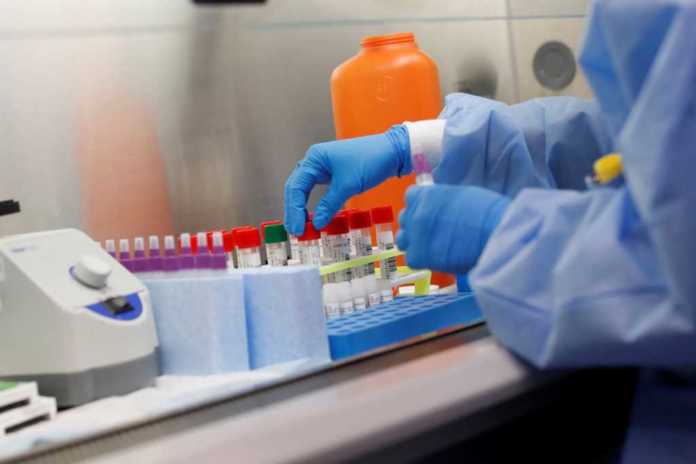
Los reguladores de salud de Estados Unidos autorizaron al gigante de diagnósticos Roche Holding AG, una aprobación de emergencia para una prueba automatizada de coronavirus.
Esta nueva prueba aceleraría en diez veces la capacidad de evaluar a los pacientes, ayudando a resolver un obstáculo significativo para los esfuerzos estadounidenses para contener el virus.
La Administración de Drogas y Alimentos (FDA, en inglés) otorgó una “autorización de uso de emergencia” para la prueba, que funciona en los sistemas cobas 6800/8800 de Roche, informó.
El sistema 8800 puede evaluar hasta 4.128 pacientes por día. El sistema 6800 puede probar hasta 1.440 por día, confirmó la compañía con sede en Suiza.
“Estamos aumentando la velocidad definitivamente en un factor de 10”, dijo a Bloomberg News Thomas Schinecker, jefe de la unidad de diagnóstico de Roche.
Esta es la primera prueba disponible en el mercado con aprobación de emergencia de la FDA. La agencia aprobó las herramientas de diagnóstico de los CDC y el Departamento de Salud Pública del Estado de Nueva York el mes pasado.
Los sistemas cobas de Roche están disponibles en todo el mundo, según Bloomberg News. Hay 695 de los denominados 6800 y 132 de los 8800 disponibles. Hay 110 de estos sistemas en Estados Unidos, y la compañía dijo que instaló una “cantidad significativa” en el país durante las últimas semanas.
Los dos sistemas pueden proporcionar resultados de pruebas en cuatro horas. La compañía dijo que está “llegando a los límites de su capacidad de producción”, informó Bloomberg News. La compañía se negó a comentar sobre el precio de las pruebas en las tiendas.